
Full resolution (TIFF) - On this page / på denna sida - N:o 11. Den 17 november 1919 - Om reaktionsförmåga i fast aggregationstillstånd. Af J. Arvid Hedvall
<< prev. page << föreg. sida << >> nästa sida >> next page >>
Below is the raw OCR text
from the above scanned image.
Do you see an error? Proofread the page now!
Här nedan syns maskintolkade texten från faksimilbilden ovan.
Ser du något fel? Korrekturläs sidan nu!
This page has never been proofread. / Denna sida har aldrig korrekturlästs.
189
* D
tillräckligt hastigt för att med tillhjälp af termoelement kunna studeras
genom upphettnings- eller afkylningskurvor på samma sätt som i
metallsmältor.1 Vid upphettning t. ex. af bariumsuperoxid med olika
modifikationer af kiselsyra kunde således efter några minuter uppkomsten af
ett bariumsilikat, motsvarande en omsättning af c:a 10 %, påvisas. I
detta och flera andra undersökta system kunde en alldeles tydlig
inverkan af kornstorlek och modifikation iakttagas på temperatur-tidskurvorna,
i det att de kurvor, som motsvara blandningar af oxid och amorf
kiselsyra, förlöpte vida brantare, än de lör
motsvarande blandning med kristal- f c-
lisk kiselsyra. Detta har sin grund i,
att i förra fallet en större mängd
sili-kat bildats per tidsenhet än i det
senare. Begynnelsetemperaturerna för
reaktionen ligga i bägge fallen mycket
lagt vid c:a 300° och lägre för den
amorfa kiselsyran än för den kri- ^
stalliniska. Förvånande hastiga reak- £
tionsförlopp och låga begynnelse- ^
temperaturer ha iakttagits vid upp- <\
hettning af barium superoxid med
diverse andra oxider och med
sulfider. De flesta oxider sönderdela * | /b
barium superoxid katalytiskt redan
vid så låga temperaturer som c:a 200°
eller till och med ännu lägre. Upp.
hettas bariumsuperoxid med t. ex
kopparoxidul sker oxidationen till
kopparoxid med stor hastighet
redan under 200°. Med de flesta sura oxider reagerar barium superoxiden
på liknande sätt till saltartade föreningar. Reaktionen kan därvid som
t. ex. med arseniktrioxid förlöpa i två stadier: oxidation af den sura
oxiden (As208-As205) till en högre oxid och den senares omsättning med
den bildade bariumoxiden. Föreligger den sura oxiden redan från början
på högsta mättningsstadiet sker vanligen först en katalytisk sönderdelning
af bariumsuperoxiden och den uppkomna bariumoxiden reagerar hastigt
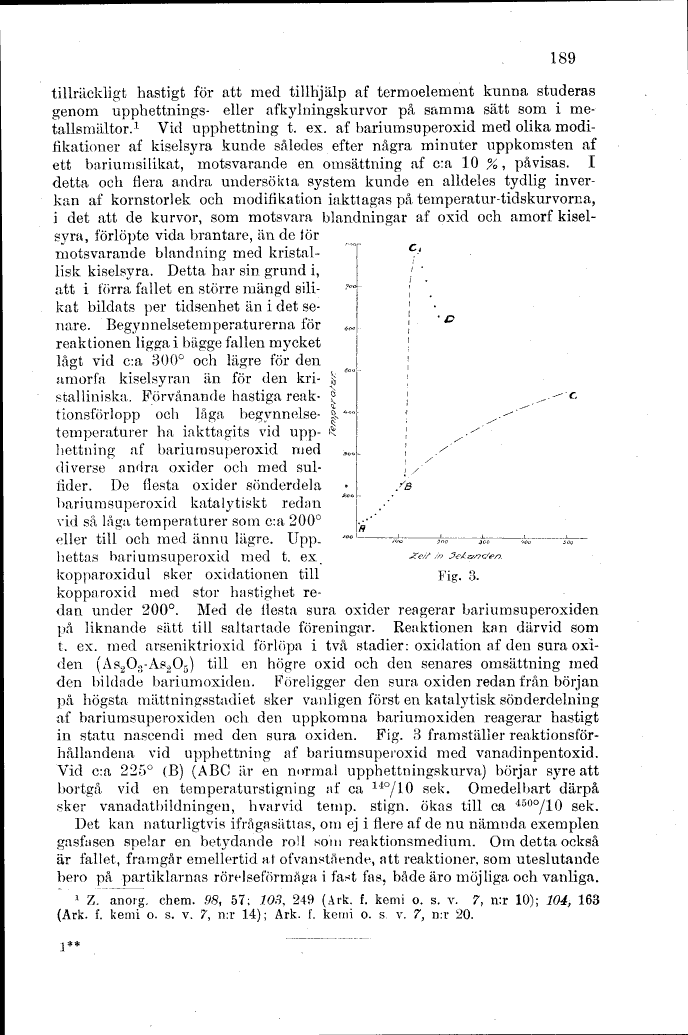
in statu nascendi med den sura oxiden. Fig. 3 framställer
reaktionsför-hållandena vid upphettning af bariumsuperoxid med vanadinpentoxid.
Vid c:a 225° (B) (ABC är en normal upphettningskurva) börjar syre att
bortgå vid en temperaturstigning af ca 14°/10 sek. Omedelbart därpå
sker vanadatbildningen, hvarvid temp. stign. ökas till ca 450°/10 sek.
Det kan naturligtvis ifrågasättas, om ej i flere af de nu nämnda exemplen
gasfasen spelar en betydande roli som reaktionsmedium. Om detta också
är fallet, framgår emellertid at ofvanstående, att reaktioner, som uteslutande
bero på partiklarnas rörelseförmåga i fast fas, både äro möjliga och vanliga.
1 Z. anorg. chem. 98, 57; 103, 249 (Ark. f. kemi o. s. v. 7, n:r 10); 104, 163
(Ark. f. kemi o. s. v. 7, n:r 14); Ark. f. kemi o. s. v. 7, n:r 20.
3eAas?</en.
1 **
Fig. 3.
<< prev. page << föreg. sida << >> nästa sida >> next page >>